咨询电话:010-67862040
▎导读
慢粒是慢性粒细胞白血病(chronic myeloid leukemia, CML)的简称,也叫慢性髓性白血病,属于血液系统的恶性肿瘤,占成年白血病患者的15%,全球年发病率为1.6~2/10万。它的发病是由患者体内第9号和22号染色体末端异位产生的BCR-ABL1融合基因所致,这也是国际慢粒日定在9月22日的原因,今年是第13个国际慢粒日。

▎慢粒成为可治、可控的“慢性疾病”
慢粒(CML)虽是一种造血系统的恶性肿瘤,但自从有了酪氨酸激酶抑制剂(TKI)以来,其疗效有了跨越性的改变,明显改变了CML患者的预后及患病现况,被视为像高血压、糖尿病一样,是一种可治、可控的“慢性疾病”,甚至可通过规范化治疗实现停药达到临床康复水平。
▎慢粒治疗:规范监测疗效很重要
愈来愈多的临床研究数据表明,以伊马替尼为代表的多种TKIs作为一线治疗药物使CML患者的10年生存率达85%~90%。由于TKIs疗法不能完全根除白血病克隆,最初认为治疗需要无限期持续。然而,近年来,CML患者出现了停止治疗的可能性。事实上,在临床试验和现实人群中,大约50%处于稳定深度分子缓解(DMR,MR4.0)的CML患者可以安全地停止TKI治疗,而不会出现分子复发,从而进入无治疗缓解(treatment free remission,TFR)。
TKIs治疗获得持续的深度分子学缓解(DMR)超过2年的患者,部分能够获得长期的无治疗缓解,即功能性治愈。功能性治愈成为越来越多CML患者追求的治疗目标。需要注意的是,停药对DMR水平、停药后监测以及随访具有严格的要求,建议在专业医师指导下进行。
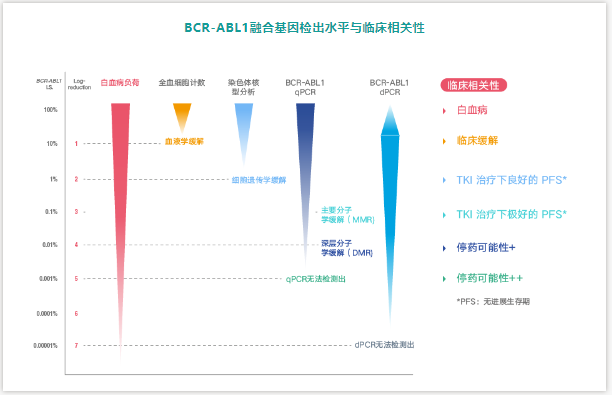
▎dPCR助力DMR患者稳定、可靠监测
随着对CML患者BCR-ABL1转录本监测的要求越来越高,分子技术在量化BCR-ABL1转录本方面的作用变得越来越重要,而细胞遗传学分析方法因敏感性较低且提供信息不足等因素,其使用逐步在减少。
实时定量PCR(qPCR)是常用的方法,但由于其固有的技术差异,在定量准确性方面存在局限性。尤其在CML患者DMR水平的监测中,多项研究表明,qPCR的敏感性不足以可靠地量化深度分子反应(DMR)患者中残留的低水平BCR-ABL1,这些患者可能有机会尝试停止酪氨酸激酶抑制剂(TKI)治疗。治疗方案依赖于每个里程碑时间点所测得的BCR-ABL1融合比值,因此必须精确测量BCR-ABL1水平。
dPCR提高了DMR准确定量和CML患者TKI停药时机把控
Goh等人表述对入组CML患者(n=112)接受一线伊马替尼治疗,在TKI停药前至少18个月通过qPCR检测不到MRD (MR4.0或更高)。尽管qPCR结果阴性,但近25%的患者dPCR结果呈阳性。dPCR阳性组复发率高于dPCR阴性组,NPV为57% (p= 0.002)。
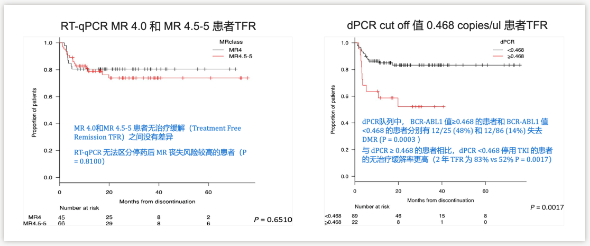
Bernardi等人评估了dPCR在MRD监测中的作用及其对持续TFR的预测价值。所有纳入的患者持续DMR为MR4.0或更高至少2年,并接受TKI治疗或中位治疗99个月。他们追踪了111名在临床试验和现实实践中尝试停用TKI的患者,用dPCR将他们分为2个DMR类别,ROC分析临界值为0.468 BCR-ABL1 拷贝/ml。DMR高于该临界值的患者复发率比低于该临界值的患者具有更高的复发率:DMR < 0.468copies/ml 的持续 TFR 的 NPV 为 86%,而当 >0.468copies/ml 时,持续TFR 的NPV为52%(p=0.0003)。
dPCR可在疾病不同程度上实现BCR-ABL1绝对定量,具有极高的精确度,临床灵敏度至少可达MR5.0,在DMR监测上,具有明显的优势。此外,dPCR已在多项研究中被验证为成功停止TKI治疗的预后标志,而使用经典qPCR却无法实现。因此,dPCR可能是前瞻性可靠地识别患者在开始TKI治疗后达到治疗里程碑以及选择TKI停药时机的首选方法。

参考文献:
1.Kockerols, C. C. B. et al. Digital PCR for BCR-ABL1 Quantification in CML: Current Applications in Clinical Practice. Hemasphere 4, e496, doi:10.1097/HS9.0000000000000496 (2020).
2.S. Bernardi et al., Digital PCR improves the quantitation of DMR and the selection of CML candidates to TKIs discontinuation. Cancer Med 8, 2041-2055 (2019).

